 |
フィレンツェ(イタリア)、ニューヨーク, 2023年12月12日 /PRNewswire/ -- 国際的な大手製薬・診断薬企業Menarini Group(「Menarini」)と、Menarini Groupの100%子会社で、がん患者に画期的な腫瘍治療を届けることに注力しているStemline Therapeutics, Inc.(「Stemline」)は、ORSERDU(R)(エラセトラント)を他の治療法と組み合わせて評価する第1b/2相臨床試験ELEVATEおよびELECTRAの結果を発表しました。ELEVATEと ELECTRAの両試験はいずれも、さまざまな治療抵抗性メカニズムを克服し、経口剤と経口剤の併用療法で患者転帰の向上を図ることを目的として設計されました。データは、2023年12月5-9日に開催された2023年サンアントニオ乳がんシンポジウム(SABCS)で発表されました。
ELEVATE試験は、PI3K/ACT/mTORパスウェイ阻害剤(エベロリムス、アルペリシブ)および細胞周期パスウェイ阻害剤(パルボシクリブ、リボシクリブ、アベマシクリブ)との併用療法でエラセストラントを評価しています。SABCS2023で報告された結果には、本試験の第1b相患者群1の全併用データが含まれており、本治療法は先行試験と一致する予測可能な安全性プロファイルを示しました。現在、薬物動態(PK)を評価し、各併用療法の推奨第2相用量(RP2D)を決定するため、追加患者群の評価が行われています。抄録の全文(1576517)は、こちらからご覧いただけます。
カリフォルニア大学サンフランシスコ校ヘレン・ディラー・ファミリー総合がんセンター血液・腫瘍内科教授のHope Rugo医学博士は「ORSERDUのさまざまな併用試験で良好な初期安全性結果が得られ、これらの試験で有望な暫定有効性データも得られたことに意を強くしています」「併用療法におけるORSERDUの役割と、転移性乳がん領域全体にわたる可能性について、さらに多くのことを学べると期待しています」と語っています。
ELECTRA試験は、アベマシクリブとの併用療法でエラセトラントを評価しています。本試験の第1b相では、転移部位に関わらず、本併用療法の推奨第2相用量(RP2D)が決定されます。両化合物はいずれも血液脳関門を通過する能力が実証されているため、第2相試験では、脳転移のあるER陽性/HER2陰性の進行性・転移性乳がん患者で本併用療法のメリットを評価する予定です。SABCS 2023で報告された結果には、第1b相試験の3つの用量患者群が含まれ、転移部位に関わらず、これらの患者群では忍容性および管理可能な安全性プロファイルが示され、暫定的な有効性も良好でした。3つの患者群は、用量制限毒性を示した患者を出さずに試験を完了しました。毒性により観察期間を超えて投与を中止した患者はいませんでした。最も一般的な有害事象は下痢、吐き気、好中球減少症/好中球数の減少でした。本併用療法では、好中球減少症のみがグレード3の有害事象と関連しており、アベマシクリブの標準的な減量で管理されました。抄録の全文(1576518)は、こちらからご覧いただけます。
Menarini GroupのElcin Barker Ergun最高経営責任者(CEO)は「ER陽性の転移性乳がん患者は治療抵抗性に直面していることが多く、革新的かつ新しい選択肢のニーズが大きい理由となっています」「今回のデータは暫定的なものですが、私たちは他の治療法との併用によるORSERDUの包括的な研究を進め、この疾患を患う人たちの延命と生活の改善を目指し、患者さんの転帰向上に取り組んでいきます」と語っています。
SABCSでのMenarini Group/Stemline Therapeuticsの発表全体の詳細については、こちらをご覧ください。
▽エラセストラント臨床開発プログラムについて
エラセトラントは、転移性乳がん疾患を対象としたいくつかの臨床試験でも、単剤療法または他の治療法との併用療法として研究が行われています。ELEVATE(NCT05563220)は、アルペリシブ、エベロリムス、パルボシクリブ、アベマシクリブ、リボシクリブとの併用によるエラセトラントの安全性と有効性を評価する、第1b/2相臨床試験です。ELECTRA(NCT05386108)は、ER陽性/HER2陰性の乳がん患者を対象にアベマシクリブとの併用療法でエラセトラントを評価する非盲検・多施設・第1b/2相試験です。第2相部分では、脳転移のある同患者集団でこの治療計画を評価しています。ELCIN(NCT05596409)は、エストロゲン受容体陽性(ER+)/ヒト上皮細胞増殖因子受容体2陰性(HER2-)の進行/転移性乳がん患者で、以前に1回または2回のホルモン療法を受け、 転移した状態でサイクリン依存性キナーゼ(CDK)4およびCDK6阻害剤(CDK4/6i)を使用したことのない人を対象にエラセトラントの有効性を評価する第2相試験です。エラセストラントは、早期乳がんを対象とした評価も行われています。
▽ORSERDU(エラセストラント)について
米国での適応症: ORSERDU(エラセストラント)345mg錠は、エストロゲン受容体(ER)陽性、ヒト上皮細胞増殖因子受容体2(HER2)陰性で、ESR1遺伝子変異のある進行性または転移性乳がんを患い、内分泌療法を少なくとも1回受けた後に病態進行した閉経後女性および成人男性の治療に適応されます。
米国向け処方情報の全文は、www.orserdu.com でご覧いただけます。
重要な安全性情報
警告および注意事項
脂質異常症: ORSERDU服用中の患者の高コレステロール血症および高トリグリセリド血症の発現率は、それぞれ30%、27%だった。グレード3および4の高コレステロール血症および高トリグリセリド血症の発現率はそれぞれ0.9%、2.2%だった。ORSERDU服用開始前および服用中は、定期的に脂質プロファイルをモニターすること。
胚・胎児毒性: 動物における所見とその作用機序から、ORSERDUは妊婦に投与すると胎児に害を及ぼす可能性がある。妊婦および生殖可能な女性には、胎児への潜在的リスクについて助言すること。生殖可能な女性には、ORSERDUによる治療中および最終投与後1週間は効果的な避妊を行うよう助言すること。生殖可能な女性パートナーがいる男性患者には、ORSERDUによる治療中および最終投与後1週間は効果的な避妊を行うよう助言すること。
副作用
ORSERDUを投与された患者の12%に重篤な副作用が発現した。ORSERDUを投与された患者の1%以上に発現した重篤な副作用は、筋骨格痛(1.7%)および吐き気(1.3%)だった。ORSERDUを投与された患者の1.7%に致命的副作用が認められ、内訳は心停止、敗血性ショック、憩室炎、原因不明(各1例)だった。
臨床検査値異常を含む、ORSERDUの最も一般的(10%以上)な副作用は、筋骨格痛 (41%)、吐き気(35%)、コレステロール増加(30%)、AST増加(29%)、トリグリセリド増加(27% 、疲労(26%)、ヘモグロビン減少(26%)、嘔吐(19%)、ALT増加(17%)、ナトリウム減少(16%)、クレアチニン増加(16%)、食欲減退(15%)、下痢 (13%)、頭痛(12%)、便秘(12%)、腹痛(11%)、ほてり(11%)、消化不良(10%)だった。
薬物相互作用
CYP3A4誘導剤と阻害剤、またはそのいずれかとの併用:強度または中等度のCYP3A4阻害剤とORSERDUとの併用は避けること。強度または中等度のCYP3A4誘導剤とORSERDUとの併用も避けること。
特定患者集団への使用
授乳:授乳中の女性は、ORSERDUによる治療中およびORSERDUの最終投与後1週間は授乳しないよう助言すること。
肝障害:重度の肝障害(Child-Pugh C)のある患者へのORSERDU投与は避けること。中等度の肝障害(Child-Pugh B)のある患者にはORSERDUの投与量を減らすこと。
小児患者でのORSERDUの安全性、有効性は確立されていません。
副作用の疑いの報告は、Stemline Therapeutics, Inc.(1-877-332-7961)またはFDA(1-800-FDA-1088 またはwww.fda.gov/medwatch )にご連絡ください。
▽Menarini Group(メナリニ・グループ)について
Menarini Groupは、売上高44億ドル超、従業員数は1万7000人を超える国際的な大手医薬品・診断薬企業です。Menariniは、満たされていないニーズの高い治療分野に重点を置き、心臓疾患、腫瘍、呼吸器疾患、消化器疾患、感染症、糖尿病、炎症、鎮痛用の製品を提供しています。18の生産拠点と9の研究開発センターを有するMenariniの製品は、世界140カ国で販売されています。詳細については、www.menarini.com をご覧ください。
▽Stemline Therapeutics Inc.について
Menarini Groupの100%子会社Stemline Therapeutics, Inc.(「Stemline」)は、新規腫瘍治療薬の開発、商品化に注力している商業期バイオ医薬品企業です。Stemlineは、エストロゲン受容体(ER)陽性、ヒト上皮細胞増殖因子受容体2(HER2)陰性でESR1遺伝子変異のある進行性または転移性乳がん患者で、内分泌療法を少なくとも1回受けた後に病態進行した閉経後女性および成人男性用の経口内分泌治療薬ORSERDU(R)(エラセストラント)を米国と欧州連合(EU)で商品化しています。Stemlineは、米国および欧州で侵攻性血液がんである芽球性形質細胞様樹状細胞腫瘍(BPDCN)患者向けにCD123を標的とする新規標的治療薬ELZONRIS(R)(タグラクソフスプ)を商品化、これは、これまでに米国およびEUで承認された唯一のBPDCN治療薬です。Stemlineは、多発性骨髄腫用のXPO1阻害剤NEXPOVIO(R)(セリネクソール)も欧州で商品化しています。Stemlineは、固形がんおよび血液がんを対象に、さまざまな開発段階にある低分子化合物およびバイオ医薬品の広範な臨床パイプラインも有しています。
Logo - https://mma.prnasia.com/media2/2296569/4449362/Menarini_Industrie_Farmaceutiche_Riunite_Logo.jpg

|
10/1 15:19 wowKorea
「ASTRO」チャウヌ、スプライトの新しいテレビ広告公開 |

|
10/1 18:01 ENCOUNT
神輿の担ぎ棒に肩が届かずまさかの“炎上”「なめてんのか?」 本人謝罪に「さすがに可哀想」の声 |

|
新着
10/2 00:39 PONY CANYON NEWS
10代のカリスマ、総SNSフォロワー600万人超えのメガインフルエンサータレントMumeixx... |

|
10/1 16:57 CNET Japan
「夕刊フジ」が休刊へ、公式サイト「zakzak」も休止 24年2月で55周年 |

|
10/1 20:25 J-CASTニュース
阪神・佐藤輝明選手が記者の質問にブチ切れ?動画が拡散 名指しされたデイリーは異例の反論、その真相は |

|
10/1 13:00 @Press
<イベント開催レポート公開>太りにくく、やせやすい体質に導く 新アプローチ『ケトン体摂取』とは... |

|
新着
10/2 12:30 共同通信
福音館書店、「母の友」休刊へ 1953年創刊、育児誌の先駆け |

|
10/1 19:10 SmartFLASH
清水アキラの“お騒がせ息子”が今度は「首グニャリで救急搬送」事故動画を自ら拡散しドン引きする人多数 |
|
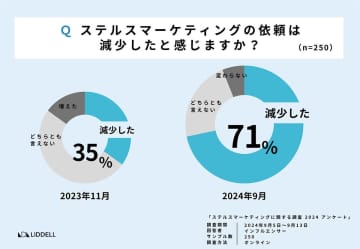
10/1 09:32 イチオシ
人気インフルエンサーの約7割が『ステマ依頼の減少』を実感、それでもステマはなくならない現実 |

|
10/1 17:02 ENCOUNT
夕刊フジ、休刊決定 押し寄せる時代の波…理由はデジタル端末の普及、購読機会の減少、コストの上昇など |

|
新着
10/2 09:45 文化放送
「夕刊フジ」が来年1月で休刊へ。森永康平氏も時代の流れに思いを馳せる |

|
10/1 15:19 共同通信
夕刊フジが休刊 |